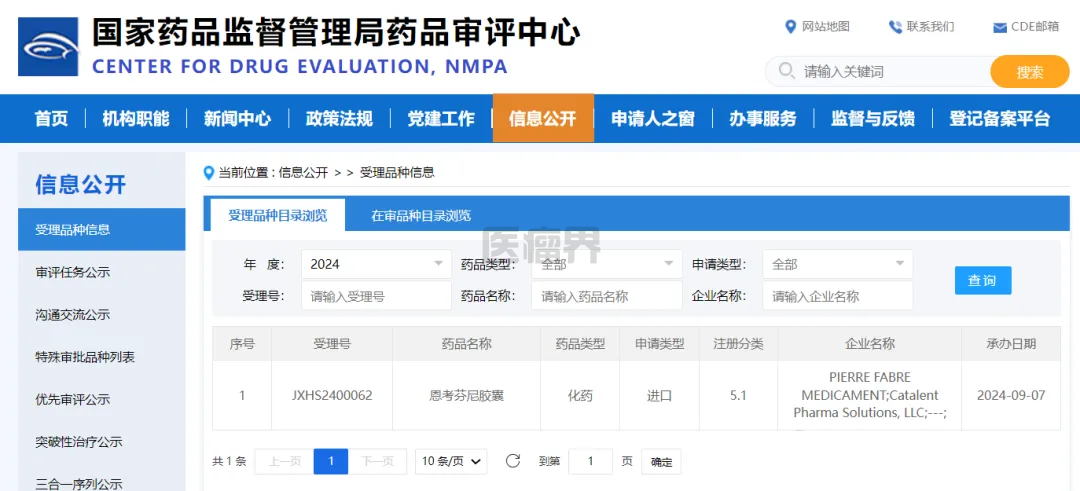
近日,国家药品监督管理局网站显示,PD-1/VEGF双特异性抗体依沃西单抗注射液(商品名:依达方)已被纳入优先审评,用于经国家药品监督管理局批准的检测方法评估为PD-L1阳性的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌(NSCLC)的一线治疗。这是依沃西单抗第二个被授予优先审评资格的适应症,这表示依沃西单抗的临床价值得到的广泛认可。
依沃西单抗注射液是一种靶向结合人血管内皮生长因子-A(VEGF-A)和程序性死亡蛋白-1(PD-1)的IgG1亚型人源化双特异性抗体,于5月24日获得国家药品监督管理局批准上市,用于联合培美曲塞和卡铂治疗经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者。
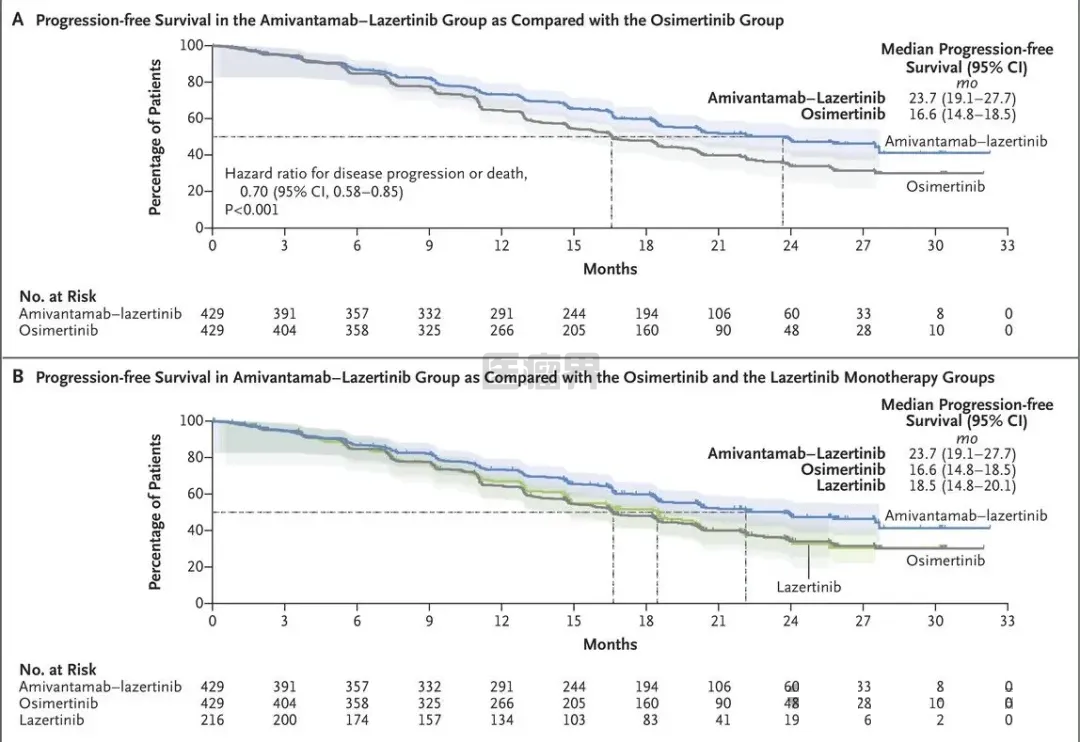
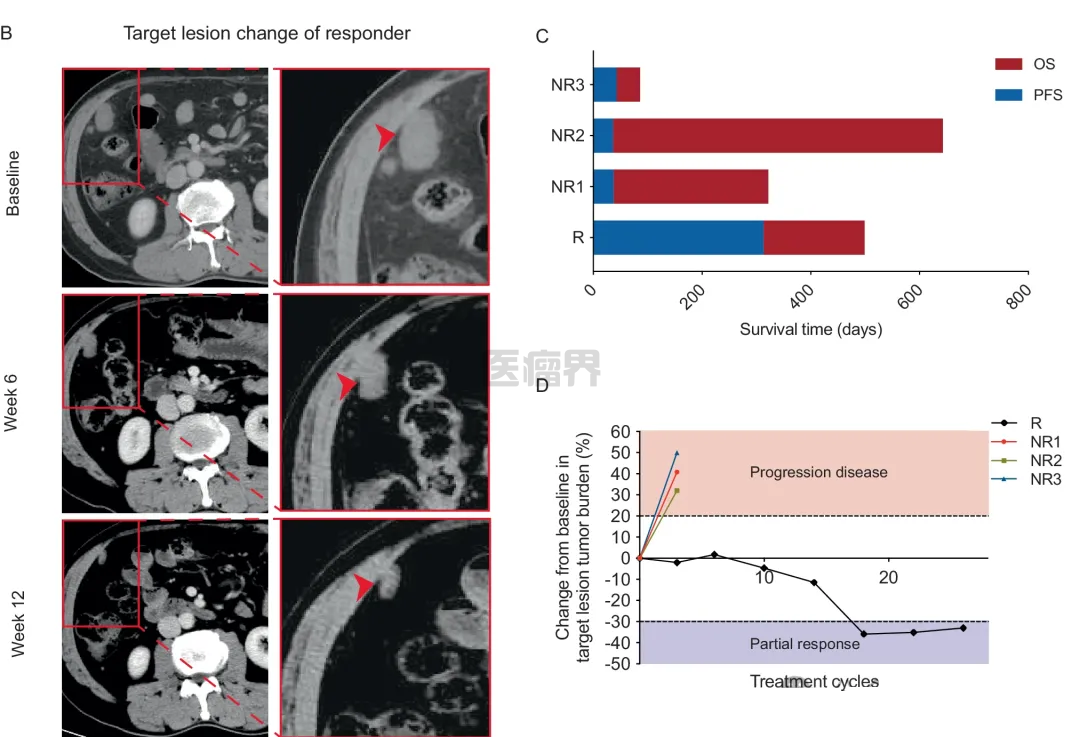
依沃西单抗的临床试验数据

截图来源于ASCO
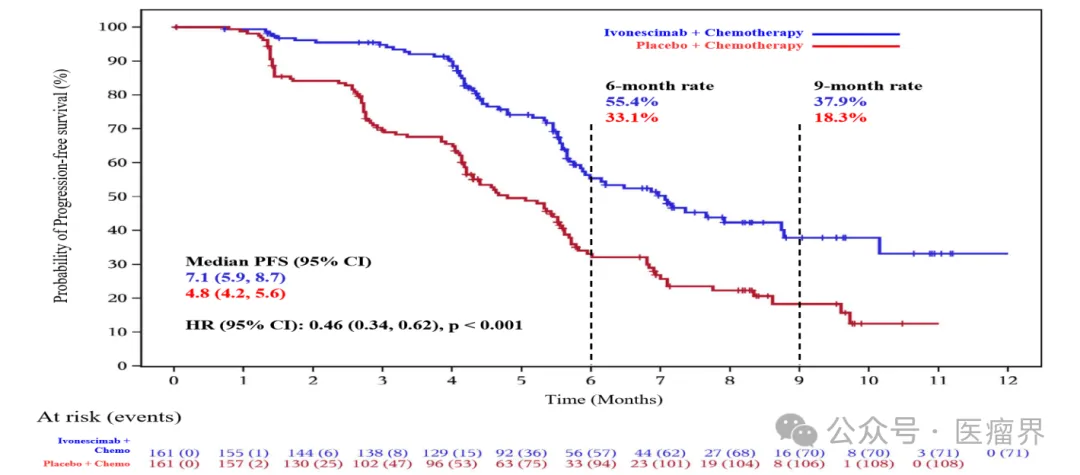
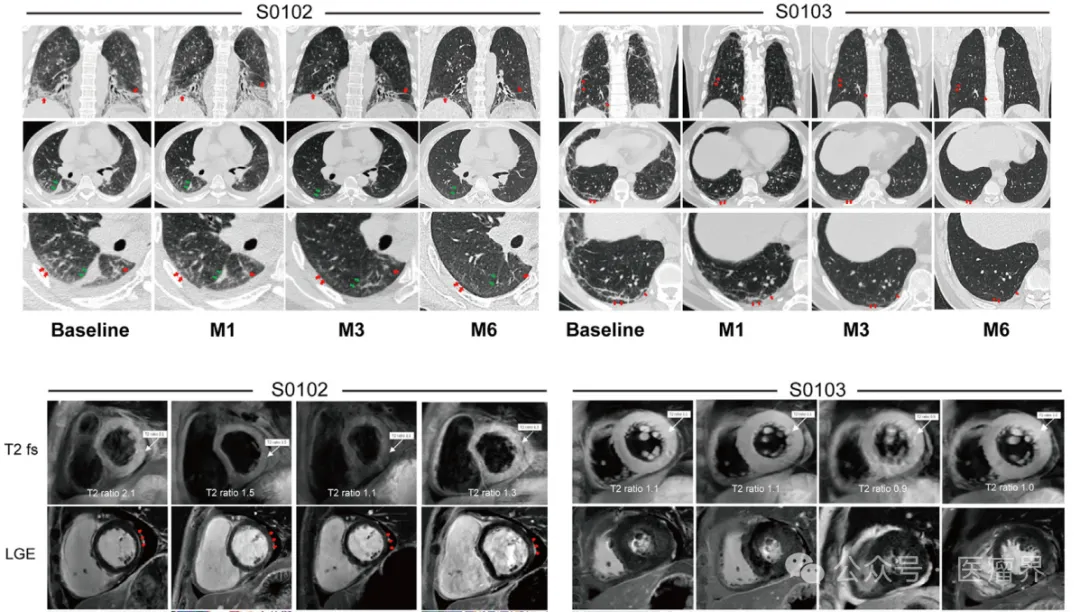
截图来源于参考资料2,侵权请联系删除
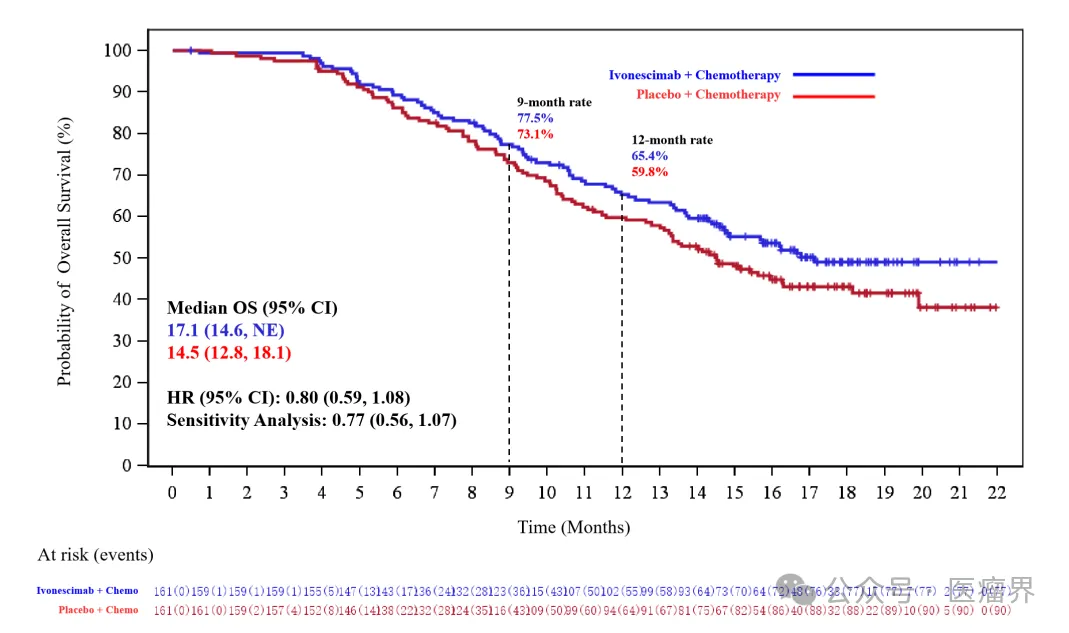
截图来源于参考资料2,侵权请联系删除



参考资料
1.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.8508
2.https://www.smmttx.com/wp-content/uploads/2024/06/Dr-Zhang_AK112-301_2024_ASCO_Oral-Presentation.pdf
3.https://ascopubs.org/doi/10.1200/JCO.2023.41.16_suppl.9114
4.https://www.jto.org/article/S1556-0864(22)00267-2/fulltext